Capreomycin Sulfate
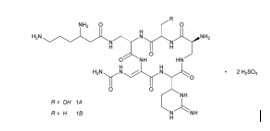
Kapreomisin sulfat [1405-37-4]
Kapreomisin 1A (basa bebas)
C25H44N14O8 BM 668,71
Kapreomisin 1B (basa bebas)
C25H44N14O7 BM 652,71
Kapreomisin Sulfat adalah garam kapreomisin disulfat, sebuah campuran polipeptida yang dihasilkan oleh Streptomyces capreolus, sesuai untuk penggunaan parenteral. Kapreomisin Sulfat mempunyai potensi setara dengan tidak kurang dari 700 µg per mg dan tidak lebih dari 1050 µg per mg kapreomisin.
Pemerian Serbuk amorf; putih atau praktis putih.
Kelarutan Sangat mudah larut dalam air; praktis tidak larut dalam pelarut organik.
Baku pembanding Kapreomisin Sulfat BPFI; lakukan pengeringan dalam hampa udara dengan tekanan tidak lebih dari 5 mmHg pada suhu 100º selama 4 jam sebelum digunakan. Simpan dalam wadah tertutup rapat, terlindung cahaya, dalam lemari pendingin. Bersifat higroskopis. Setelah wadah dibuka, simpan dalam desikator. Endotoksin BPFI [Catatan Bersifat pirogenik, penanganan vial dan isi harus hati-hati untuk menghindari kontaminasi.] Rekonstitusi semua isi, simpan larutan dalam lemari pendingin dan gunakan dalam waktu 14 hari. Simpan vial yang belum dibuka dalam lemari pembeku.
Identifikasi
A. Menunjukkan reaksi Sulfat seperti tertera pada Uji identifikasi umum <291>.
B. Waktu retensi puncak utama kromatogram Larutan uji sesuai dengan Larutan kesesuaian sistem seperti yang diperoleh pada uji Kapreomisin 1.
Endotoksin bakteri <201> Tidak lebih dari 0,35 unit Endotoksin FI per mg kapreomisin jika digunakan untuk sediaan injeksi.
pH <1071> Antara 4,5 dan 7,5; lakukan penetapan menggunakan larutan zat 30 mg per mL.
Susut pengeringan <1121> Tidak lebih dari 10,0%; lakukan pengeringan menggunakan 100 mg zat dalam hampa udara pada suhu 100° selama 4 jam.
Sisa pemijaran <301> Tidak lebih dari 3,0%. Sisa pengarangan dibasahi dengan 2 mL asam nitrat P dan 5 tetes asam sulfat P.
Logam berat <371> Metode III Tidak lebih dari 30 bpj.
Syarat lain Jika pada etiket tertera kapreomisin sulfat steril, memenuhi syarat seperti tertera pada Injeksi.
Kapreomisin 1 Tidak kurang dari 90%. Lakukan penetapan dengan cara Kromatografi cair kinerja tinggi seperti tertera pada Kromatografi <931>.
Larutan A Buat larutan amonium bisulfat 0,4 mg per mL. Saring melalui penyaring yang sesuai dengan porositas 0,5 ?m atau lebih halus.
Fase gerak Buat campuran metanol P-Larutan A (2:3), saring dan awaudarakan. Jika perlu lakukan penyesuaian menurut Kesesuaian sistem seperti tertera pada Kromatografi <931>.
Larutan kesesuaian sistem Timbang saksama sejumlah Kapreomisin Sulfat BPFI. Masukkan ke dalam labu tentukur yang sesuai. Larutkan dan encerkan dengan air hingga kadar lebih kurang 0,25 mg per mL.
Larutan uji Timbang saksama sejumlah zat, larutkan, dan encerkan dengan air hingga kadar lebih kurang 0,25 mg per mL.
Sistem kromatografi Kromatograf cair kinerja tinggi dilengkapi dengan detektor 268 nm dan kolom 4,6 mm × 25 cm berisi bahan pengisi L10 dengan ukuran partikel 5 mm. Pertahankan suhu kolom pada 30°. Laju alir lebih kurang 1,5 mL per menit. Waktu eluasi 5 kali waktu retensi puncak kapreomisin 1A. Lakukan kromatografi terhadap Larutan kesesuaian sistem, rekam kromatogram, dan ukur respons puncak seperti yang tertera pada Prosedur: waktu retensi relatif kapreomisin 1A dan kapreomisin 1B berturut-turut adalah lebih kurang 0,85 dan 1,0; resolusi, R, antara puncak kapreomisin 1A dan kapreomisin 1B tidak kurang dari 1,5 dan faktor ikutan puncak utama (kapreomisin 1A dan kapreomisin 1B) tidak lebih dari 3,5.
Prosedur Suntikkan lebih kurang 20 µL Larutan uji ke dalam kromatograf. Rekam kromatogram dan ukur semua respons puncak. Hitung persentase kapreomisin 1 dalam kapreomisin sulfat yang digunakan dengan rumus:
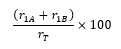
r1A dan r1B berturut-turut adalah respons puncak kapreomisin 1A dan kapreomisin 1B; rT adalah jumlah semua respons puncak.
Penetapan kadar Lakukan penetapan seperti tertera pada Penetapan Potensi Antibiotik secara Mikrobiologi <131>.
Wadah dan penyimpanan Dalam wadah tertutup rapat.
Penandaan Jika digunakan untuk pembuatan sediaan injeksi, pada etiket harus dinyatakan steril atau memerlukan proses sterilisasi untuk pembuatan sediaan injeksi.
